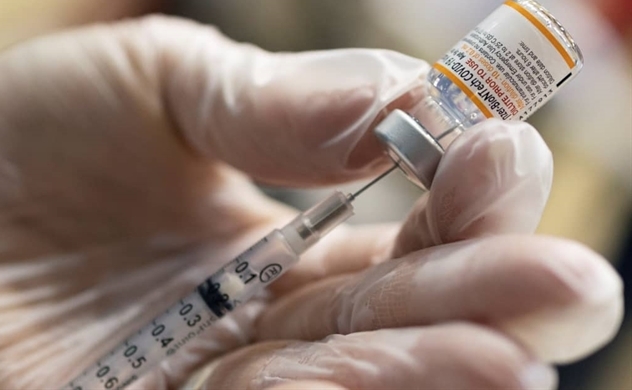
Các nghiên cứu đang được tiến hành với tốc độ nhanh chóng nên các công ty sẽ chờ đợi dữ liệu đầy đủ của cả 3 mũi vaccine.
Pfizer hoãn đăng ký tiêm vaccine cho trẻ em dưới 5 tuổi
Pfizer và BioNTech cho biết họ đang trì hoãn việc xin Cục Quản lý Thực phẩm và Dược phẩm (FDA) cấp phép cho vaccine COVID-19 dành cho trẻ em dưới 5 tuổi cho đến đầu tháng 4, chờ thêm dữ liệu về hiệu quả của mũi thứ ba.
Các nghiên cứu đang được tiến hành với tốc độ nhanh chóng nên các công ty sẽ chờ đợi dữ liệu đầy đủ của cả 3 mũi vaccine. Pfizer và BioNTech đều tin rằng có thể cung cấp mức độ bảo vệ cao hơn ở nhóm tuổi này. Pfizer cần thêm dữ liệu vì biến thể Omicron gây ra tỷ lệ nhiễm trùng và bị ốm vẫn còn cao ở trẻ em dưới 5 tuổi.
Việc trì hoãn gây không ít thất vọng cho các bậc cha mẹ đang nóng lòng chờ đợi cơ hội tiêm vaccine cho con mình. Trẻ em dưới 5 tuổi là nhóm tuổi cuối cùng còn lại ở Hoa Kỳ không đủ điều kiện để tiêm chủng.
 |
| Em Brayden Burton, 3 tuổi, đang được điều trị COVID-19 tại Bệnh viện Nhi Georgia ở Augusta, Georgia, Hoa Kỳ. Ảnh: Reuters. |
Tiến sĩ Peter Marks, người đứng đầu bộ phận chịu trách nhiệm về an toàn vaccine của FDA, cho biết tốt hơn hết nên đợi thêm thông tin và dữ liệu của mũi tiêm thứ 3 để thẩm định và đảm bảo rằng vaccine an toàn và hiệu quả cho trẻ em. Ông hy vọng điều này sẽ trấn an mọi người rằng mọi quyết định của cơ quan đều tuân theo quy trình có tiêu chuẩn và khoa học.
Ông Marks cho biết các bậc cha mẹ trước mắt sẽ phải dựa vào các biện pháp phòng tránh để bảo vệ con cái trong khi chờ đợi vaccine được phê duyệt. Các biện pháp đó bao gồm đeo khẩu trang và đảm bảo rằng mọi thành viên trong gia đình đều đã được tiêm chủng.
Các cơ quan quản lý y tế Hoa Kỳ đã phải đối mặt với áp lực phê duyệt việc tiêm vaccine ngày càng tăng của công chúng, khi số trẻ em nhập viện đã tăng lên mức kỷ lục do biến chủng Omicron gây ra. FDA ban đầu đã yêu cầu Pfizer và BioNTech gửi yêu cầu cấp phép cho hai liều vaccine đầu tiên, trong khi họ hoàn thành việc thu thập dữ liệu về hiệu quả của liều thứ ba.
Pfizer và BioNTech, theo yêu cầu của FDA, đã đệ trình đơn xin cấp phép hai liều đầu tiên vào tuần trước, với lý do nhu cầu sức khỏe cộng đồng khẩn cấp cho trẻ nhỏ hơn 5 tuổi. Tuy nhiên, Giám đốc điều hành Pfizer, ông Albert Bourla cho biết vào thời điểm đó, trẻ em dưới 5 tuổi vẫn sẽ cần liều thứ ba để có mức độ bảo vệ cao nhất chống lại Omicron và các biến thể trong tương lai.
Pfizer đã sửa đổi thử nghiệm lâm sàng cho trẻ em vào tháng 12 để nghiên cứu mũi thứ ba sau khi hai liều đầu tiên không tạo ra phản ứng miễn dịch đầy đủ ở trẻ từ 2 đến 4 tuổi. Trẻ nhỏ hơn sẽ được tiêm liều lượng ít hơn, 3 microgram, so với các mũi tiêm 30 microgram được chấp thuận cho người lớn.
Tháng trước, cố vấn y tế của Nhà Trắng, Tiến sĩ Anthony Fauci cho biết ông hy vọng FDA sẽ mở rộng điều kiện sử dụng vaccine cho trẻ em vào tháng Hai.
Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh (CDC) đã bắt đầu đặt cơ sở để phân phối các mũi tiêm trong tháng này, thông báo với các quan chức y tế địa phương và tiểu bang vào đầu tuần này rằng họ có thể nhận được lô hàng đầu tiên trước ngày 21 tháng 2. Tuy nhiên, CDC cho biết lô hàng sẽ chỉ bắt đầu được phân phối khi FDA cấp phép cho vaccine.
CDC có kế hoạch tung ra 10 triệu liều trong ba giai đoạn ngay sau khi FDA cho phép tiêm Pfizer và BioNTech cho trẻ em từ 6 tháng đến 4 tuổi. Các quan chức y tế của tiểu bang và địa phương đã có thể bắt đầu đặt hàng trước những liều thuốc đầu tiên.
Có thể bạn quan tâm:
Ngành công nghiệp thẩm mỹ "bùng nổ" sau đại dịch
Nguồn CNBC

 English
English


_71049984.png)




_21258127.png?w=158&h=98)
_81523335.png?w=158&h=98)
_61041843.png?w=158&h=98)




